Разнообразные виды изомерии в органической химии: взаимосвязь структуры молекул с физическими и химическими свойствами веществ

Изомерия - удивительное явление в органической химии, позволяющее существовать веществам одинакового состава, но с разными свойствами. Давайте разберемся в многообразии видов изомерии и откроем для себя это захватывающее разнообразие органических соединений!

Структурная изомерия
Структурная изомерия возникает из-за разного порядка соединения атомов в молекуле органических соединений. Это приводит к образованию веществ с одинаковым составом, но разными свойствами.
Одним из видов структурной изомерии является изомерия углеродного скелета. Рассмотрим ее на примере бутана и пентана. Для бутана C4H10 известен только один изомер с линейным расположением атомов углерода. А.М. Бутлеров предположил существование еще одного изомера бутана с разветвленным строением - изобутана. Аналогично, для пентана C5H12 возможно уже 3 изомера:
- н-пентан (неразветвленный)
- изопентан
- неопентан
Температуры кипения этих изомеров пентана различаются, что доказывает зависимость свойств веществ от строения их молекул.
Другой распространенный вид - изомерия положения. Она возникает при разном положении функциональной группы, кратной связи или заместителей в молекуле. Например, существуют изомеры по положению двойной связи в бутене-1 и бутене-2. А для спиртов возможна изомерия положения гидроксильной группы, как в случае н-пропилового и изопропилового спиртов:
Еще один тип структурной изомерии - межклассовая изомерия. Здесь вещества с одинаковым составом относятся к разным классам органических соединений. Например, к одной молекулярной формуле C2H6O относятся этанол и диметиловый эфир. Этанол проявляет кислотные свойства, а диметиловый эфир - нет. Кроме того, этанол - жидкость, а диметиловый эфир - газ.
Таким образом, наличие разных структурных изомеров в органической химии ведет к образованию соединений с разнообразными физическими и химическими свойствами.
Геометрическая изомерия
Геометрическая изомерия характерна для соединений с двойными связями или циклами. Здесь заместители при атомах углерода могут располагаться либо по одну сторону условной плоскости (цис-положение), либо по разные ее стороны (транс-положение).
Классическим примером геометрической изомерии служат малеиновая и фумаровая кислоты - цис- и транс-изомеры соответственно. У них одинаковый состав C4H4O4, но разное расположение карбоксильных групп относительно двойной связи. Это ведет к различию их свойств:
| Свойство | Малеиновая кислота (цис-форма) | Фумаровая кислота (транс-форма) |
| Температура плавления, °C | 130 | 286 |
| Растворимость в 100 г воды при 20°С, г | 78,8 | 0,7 |
Как видно из таблицы, геометрические изомеры существенно отличаются по физическим характеристикам. Они могут также по-разному вступать в химические реакции.
Между цис- и транс-формами возможны переходы при воздействии реагентов или облучения. Так, под действием йода менее стабильная форма переходит в более устойчивую. Это важно учитывать при получении и использовании геометрических изомеров на практике.
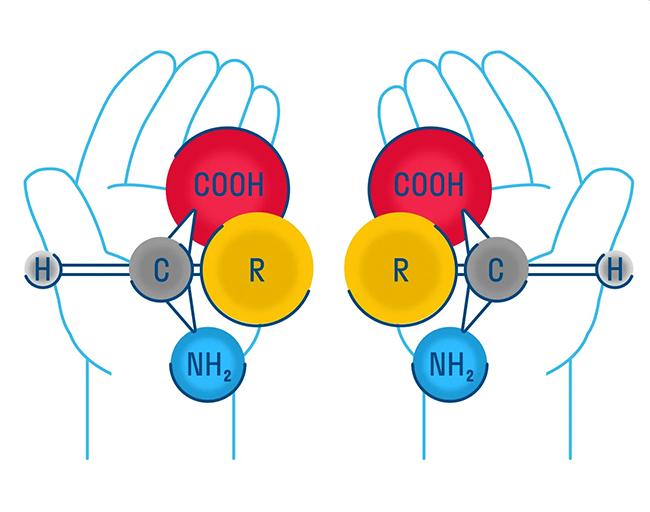
Оптическая изомерия
Еще один распространенный вид изомерии - оптическая. Она возникает, когда асимметричная молекула не совместима со своим отражением в зеркале. Такие оптические антиподы или энантиомеры обладают схожими химическими свойствами, но различаются знаком вращения плоскости поляризации света.
Ярким примером оптической изомерии является молочная кислота. Она существует в виде право- и левовращающих стереоизомеров. Их структурные формулы можно представить следующим образом:
Смесь равных количеств энантиомеров называется рацематом и не проявляет оптической активности. При химических реакциях всегда образуется рацемическая смесь, если только не использовать специальные методы разделения оптических изомеров.
Практическое значение изомерии
Наличие изомеров в органической химии имеет большое практическое значение. Во-первых, изомеры одного вещества зачастую обладают разной биологической активностью и могут по-разному влиять на живые организмы. Например, левовращающая молочная кислота участвует в обменных процессах, а правовращающая - нет.
Во-вторых, свойства изомеров активно используются в пищевой и парфюмерной промышленности для получения продукции с нужными характеристиками. Так, малиновый запах обеспечивает один геометрический изомер β-ионона, в то время как другой изомер отвечает за запах фиалки.
Методы исследования изомерии
Для определения типа изомерии вещества и структуры изомеров используется целый ряд физико-химических методов. К ним относятся:
- хроматографические методы;
- ИК-, УФ-, ЯМР-спектроскопия;
- рентгеноструктурный анализ.
Эти методы позволяют не только разделять смеси изомеров, но и определять строение каждого из них, выявлять особенности взаимного расположения атомов и заместителей.
Перспективы изучения изомерии
Несмотря на многолетнюю историю изучения, изомерия до сих пор хранит немало загадок и открытий. Например, недавно были открыты изомеры одиночных атомов, отличающиеся квантовыми состояниями. В будущем, вероятно, будут найдены новые виды изомеров, расширены представления о влиянии структуры на реакционную способность и биологическую активность.
Похожие статьи
- Информатика – это наука... Что изучает информатика?
- Подготовка к исповеди. Список грехов для исповеди
- История развития вычислительной техники. Отечественная вычислительная техника. Первая ЭВМ
- Специальность "Технология машиностроения". Кем можно работать?
- Зачем нужна география в жизни? Зачем нужно изучать географию?
- Специальность "государственное и муниципальное управление": кем потом работать?
- Парные и непарные, звонкие и глухие, мягкие и твердые согласные звуки в русском языке
