Электрохимическая коррозия и защита от нее
Коррозией называют процесс самопроизвольного разрушения поверхности материалов вследствие взаимодействия с окружающей средой. Ее причиной является термодинамическая неустойчивость химических элементов к определенным веществам. Формально коррозии подвержены полимеры, дерево, керамика, резина, но к ним чаще применяют термин «старение». Наиболее серьезный ущерб наносит ржавление металлов, для защиты которых разрабатываются высокотехнологичные контрмеры. Но об этом мы поговорим позже. Учеными различается коррозия металлов химическая и электрохимическая.

Химическая коррозия
Она возникает обычно при воздействии на металлическую структуру сухих газов, жидкостей или растворов, не проводящих электрический ток. Суть этого типа коррозии – прямое взаимодействие металла с агрессивной средой. Элементы химически корродируют во время термической обработки или в результате длительной эксплуатации при достаточно высоких температурах. Это касается лопаток газовых турбин, арматуры плавильных печей, деталей двигателей внутреннего сгорания и так далее. В результате на поверхности образуются определенные соединения: оксиды, нитриды, сульфиды.
Электрохимическая коррозия
Она является следствием контакта металла с жидкой средой, способной проводить электрический ток. Вследствие окисления материал претерпевает структурные изменения, приводящие к образованию ржавчины (нерастворимого продукта), либо частицы металла переходят в раствор ионов.
Электрохимическая коррозия: примеры
Ее разделяют на:
- Атмосферную, которая возникает при наличии на поверхности металла жидкостной пленки, в которой газы, содержащиеся в атмосфере (например, О2, СО2, SO2), способны растворяться с образованием электролитных систем.
- Жидкостную, которая протекает в токопроводящей жидкой среде.
- Грунтовую, что протекает под воздействием грунтовых вод.
Причины
Поскольку обычно любой металл, который используется для промышленных нужд, не является идеально чистым и содержит включения различного характера, то электрохимическая коррозия металлов возникает вследствие образования на поверхности железа большого количества короткозамкнутых локальных гальванических элементов.
Появление их может быть связано не только с наличием различных (особенно металлических) примесей (контактная коррозия), но и с неоднородностью поверхности, дефектами кристаллической решетки, механическими повреждениями и тому подобное.
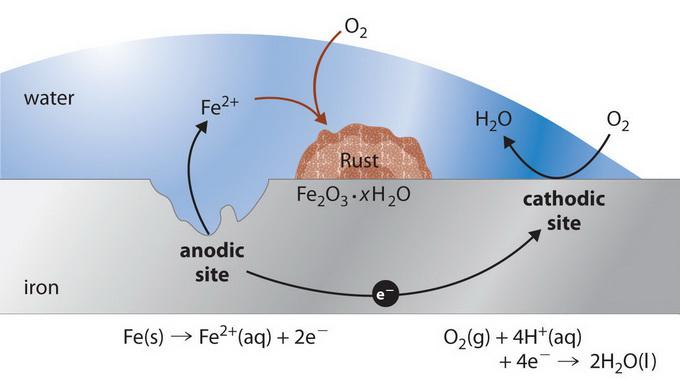
Механизм взаимодействия
Процесс электрохимической коррозии зависит от химического состава материалов и особенностей внешней среды. Если так называемый технический металл покрыт влажной пленкой, то в каждом из указанных гальванических микроэлементов, которые образуются на поверхности, протекают две независимые реакции. Более активный компонент коррозионной пары отдает электроны (к примеру, цинк в паре Zn-Fe) и переходит в жидкую среду в качестве гидратированных ионов (то есть корродирует) по следующей реакции (анодный процесс):
М + nH2O = Mz+* nH2O + ze.
Эта часть поверхности является отрицательным полюсом локального микроэлемента, где металл электрохимически растворяется.
На менее активном участке поверхности, которая является положительным полюсом микроэлемента (железо в паре Zn-Fe), электроны связываются за счет протекания реакции восстановления (катодный процесс) по схеме:
Ox + ze = Red.
Таким образом, наличие окислителей в водяной пленке, которые способны связывать электроны, обеспечивает возможность дальнейшего хода анодного процесса. Соответственно, электрохимическая коррозия может развиваться только при условии одновременного протекания как анодного, так и катодного процессов. Вследствие торможения одного из них скорость окисления уменьшается.

Процесс поляризации
Оба вышеуказанных процесса вызывают поляризацию соответствующих полюсов (электродов) микроэлемента. Какие здесь есть особенности? Обычно электрохимическая коррозия металлов более существенно замедляется поляризацией катода. Поэтому она будет усиливаться под влиянием факторов, которые предотвращают эту реакцию и сопровождаются так называемой деполяризацией положительного электрода.
Во многих коррозионных процессах катодная деполяризация осуществляется разрядом ионов водорода либо восстановлением молекул воды и соответствует формулам:
- В кислой среде: 2Н+ + 2е = Н2.
- В щелочной: 2Н2О + 2е = Н2 + 2ОН–.
Диапазон потенциалов
Потенциал, который соответствует этим процессам, в зависимости от природы агрессивной среды, может изменяться от -0,83 до 0 В. Для нейтрального водного раствора при температурах, близких к стандартной, он равен примерно -0,41 В. Следовательно, ионы водорода, содержащиеся в воде и в нейтральных водных системах, могут окислять только металлы с потенциалом, меньшим, чем -0,41 В (расположенные в ряду напряжений до кадмия). Учитывая то, что некоторые из элементов защищены оксидной пленкой, число металлов, подверженных окислению в нейтральных средах ионами водорода, незначительное.
Если влажная пленка содержит растворенный кислород воздуха, то он способен, в зависимости от характера среды, связывать электроны эффектом кислородной деполяризации. В этом случае схема электрохимической коррозии выглядит следующим образом:
- О2 + 4е + 2Н2О = 4ОН– или
- О2 + 4е + 4Н+ = 2Н2О.
Потенциалы указанных электродных реакций при температурах, близких к стандартной, изменяются от 0,4 В (щелочная среда) до 1,23 В (кислая среда). В нейтральных средах потенциал процесса восстановления кислорода при указанных условиях соответствует значению 0,8 В. Значит, растворенный кислород способен окислять металлы с потенциалом меньше 0,8 В (расположенные в ряду напряжений до серебра).

Важнейшие окислители
Виды электрохимической коррозии характеризуются окислительными элементами, важнейшими из которых являются ионы водорода и кислород. При этом пленка, содержащая растворенный кислород, в коррозионном отношении значительно опаснее, чем влага, где кислорода нет, и которая способна окислять металлы исключительно ионами водорода, так как в последнем случае количество видов материалов, способных корродировать, значительно меньше.
Например, в стали и в чугуне присутствуют примеси углерода преимущественно в виде карбида железа Fe3C. В этом случае механизм электрохимической коррозии с водородной деполяризацией для указанных металлов выглядит следующим образом:
- (-) Fe - 2e + nH2O = Fe2+· nH2O (может образовываться ржавчина);
- (+) 2Н+ + 2е = Н2 (в подкисленной среде);
- (+) 2Н2О + 2е = Н2 + 2ОН– (в нейтральной и щелочной среде).
Механизм коррозии железа, в котором содержатся примеси меди, в случае кислородной деполяризации катода описывается уравнениями:
- (-) Fe - 2e + nH2O = Fe2+·nH2O;
- (+) 0,5О2 + Н2О + 2е = 2ОН– (в подкисленной среде);
- (+) 0,5О2 + 2Н+ + 2е = Н2О (в нейтральной и щелочной среде).
Электрохимическая коррозия протекает с разной скоростью. Этот показатель зависит от:
- разности потенциалов между полюсами гальванического микроэлемента;
- состава и свойств электролитной среды (рН, наличие ингибиторов и стимуляторов коррозии);
- концентрации (интенсивности подачи) окислителя;
- температуры.
Методы защиты
Электрохимическая защита металлов от коррозии достигается следующими способами:
- Созданием антикоррозионных сплавов (легированием).
- Увеличением чистоты индивидуального металла.
- Нанесением на поверхность различных защитных покрытий.
Эти покрытия в свою очередь бывают:
- Неметаллическими (краски, лаки, смазочные материалы, эмали).
- Металлическими (анодные и катодные покрытия).
- Образованными специальной обработкой поверхностей (пассивация железа в концентрированных серной или азотной кислотах; железа, никеля, кобальта, магния в растворах щелочей; образование оксидной пленки, например, на алюминии).
Металлическое защитное покрытие
Наиболее интересной и перспективной является электрохимическая защита от коррозии другим видом металла. По характеру защитного воздействия металлизированные покрытия подразделяют на анодные и катодные. Остановимся на этом моменте более подробно.
Анодным называется покрытие, образованное более активным (менее благородным) металлом, чем тот, что защищают. То есть осуществляется защита элементом, который стоит в ряду напряжений до основного материала (например, покрытие железа цинком или кадмием). При местных разрушениях защитного слоя корродировать будет менее благородный металл-покрытие. В зоне царапин и трещин образовывается локальный гальванический элемент, катодом в котором является ограждаемый металл, а анодом – покрытие, которое окисляется. Целостность такой защитной пленки значения не имеет. Однако чем она толще, тем медленнее будет развиваться электрохимическая коррозия, дольше будет длиться полезный эффект.
Катодным называется покрытие металлом с большим потенциалом, который в ряду напряжений стоит после защищаемого материала (например, напыление низколегированных сталей медью, оловом, никелем, серебром). Покрытие должно быть сплошным, так как при его повреждении образовываются локальные гальванические элементы, в которых основной металл будет анодом, а защитный слой – катодом.

Как уберечь металл от окисления
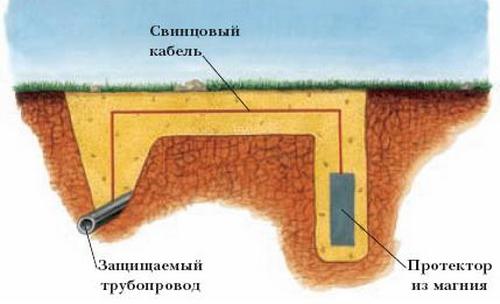
Электрохимическая защита от коррозии подразделяется на два типа: протекторную и катодную. Протекторная аналогична анодному покрытию. К материалу, который нужно защитить, присоединяют большую пластину более активного сплава. Образуется гальванический элемент, основной металл в котором служит катодом, а протектор – анодом (он корродирует). Обычно для этого типа защиты применяют цинк, алюминий или сплавы на основе магния. Протектор постепенно растворяется, поэтому его нужно периодически заменять.
Много неприятностей в коммунальном хозяйстве и в промышленности в целом доставляет электрохимическая коррозия трубопроводов. В борьбе с ней наиболее подходит метод катодной поляризации. Для этого металлическая конструкция, которая защищается от разрушительных процессов окисления, подключается к отрицательному полюсу какого-либо внешнего источника постоянного тока (она после этого становится катодом, при этом возрастает скорость выделения водорода, а скорость коррозии снижается), а к положительному полюсу присоединяют малоценный металл.
Электрохимические методы защиты эффективны в токопроводящей среде (яркий пример – морская вода). Поэтому протекторы часто используют, чтобы защитить подводные части морских судов.
Обработка агрессивной среды
Этот метод является эффективным, когда электрохимическая коррозия железа протекает в небольшом объеме токопроводящей жидкости. Справиться с разрушительными процессами в этом случае можно двумя способами:
- Удалением из жидкости кислорода (деаэрация) в результате продувки инертным газом.
- Введением в среду ингибиторов – так называемых замедлителей коррозии. Например, в случае если поверхность разрушается в результате окисления кислородом, добавляют органические вещества, молекулы которых содержат определенные аминокислоты (имино-, тио- и другие группы). Они хорошо адсорбируются на поверхности металла и существенно снижают скорость электрохимических реакций, приводящих к разрушениям поверхностного контактного слоя.
Вывод
Безусловно, коррозия химическая и электрохимическая приносит значительный ущерб и в промышленности, и в быту. Если бы металл не корродировал, срок службы многих предметов, деталей, агрегатов, механизмов значительно увеличился бы. Сейчас ученые активно разрабатывают альтернативные материалы, способные заменить металл, не уступающие по эксплуатационным характеристикам, однако полностью отказаться от его применения в ближайшей перспективе, наверное, невозможно. В этом случае на передний план выходят передовые методы защиты металлических поверхностей от коррозии.
Похожие статьи
- Что такое коррозия металла: виды, причины и методы защиты
- Удаление ржавчины с кузова автомобиля своими руками. Средство для удаления ржавчины
- Антикоррозийная обработка кузова своими руками: особенности технологии, необходимые материалы, полезные советы
- "Цинкарь" - преобразователь ржавчины. Отзывы, советы по использованию. Автохимия
- Анодирование алюминия в домашних условиях: технология процесса
- Электролиз воды: что нам о нем известно
- Электролитическая диссоциация: уравнение, степень, константа, реакции
