Молярная масса железа и описание химического элемента

Железо (Fe) имеет для человека большое значение. Этот элемент необходим как для питания растений и поддержания уровня кислорода в крови, так и промышленной сферы в качестве одного из основных материалов.
Оно представляет собой хрупкое, твердое вещество, классифицирующееся как металл в группе 8 периодической таблицы элементов. Это самый чистый из всех металлов, он сильно подвержен воздействию влажного воздуха и высоких температур.
Использование и значение
Железо является четвертым наиболее распространенным по массе элементом в земной коре, и считается, что большая часть ядра Земли состоит из него. Оно имеет решающее значение для выживания живых организмов. У растений необходим в производстве хлорофилла. У животных является компонентом гемоглобина — белка в крови, который переносит кислород из легких в ткани организма.
Твердое внутреннее и жидкое внешнее ядра Земли в основном состоят из железа (примерно 85 и 80 процентов от общей массы соответственно). Электрический ток, создаваемый жидкой его формой, формирует магнитное поле, защищающее Землю. Оно также находится в ядрах всех планет Солнечной системы.

Большая часть его используется для производства стали, сплава железа и углерода, которая, в свою очередь, используется в производстве и гражданском строительстве. Нержавеющая сталь, которая содержит не менее 10,5 % хрома, обладает высокой устойчивостью к коррозии. Ее применяют в кухонных столовых приборах и посуде. Добавление других элементов может придать другие полезные качества. Например, никель увеличивает долговечность и делает более устойчивым к теплу и кислотам; вольфрам помогает сохранять твердость при высоких температурах.
Характеристики
Основные свойства химического элемента железо:
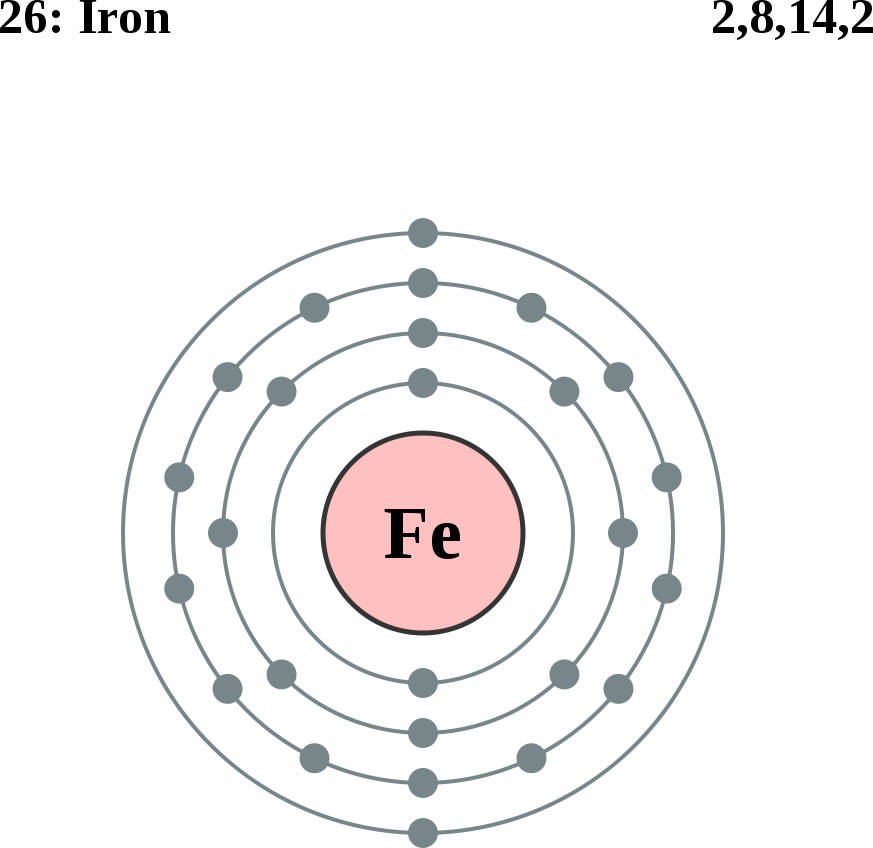
- Атомный номер (количество протонов в ядре): 26.
- Атомный символ (в периодической таблице элементов): Fe.
- Атомный вес (средняя масса атома): 55,845.
- Плотность: 7,874 грамма на кубический сантиметр.
- Состояние при комнатной температуре: твердое.
- Температура плавления: 1538° C.
- Температура кипения: 2 861° C.
- Количество изотопов (атомов одного и того же элемента с различным числом нейтронов): 33, из них стабильных – 4.
- Наиболее распространенные изотопы: железо-56
История и свойства
Археологи подсчитали, что люди используют железо более 5 000 лет. На самом деле получается, что самые древние из известных человеку образцов буквально упали с неба. В изысканиях, опубликованных в 2013 году в "Журнале археологических наук", исследователи изучили древнеегипетские бусы, датируемые примерно 3 200 г. до н. э., и обнаружили, что они были сделаны из метеоритного железа.
Его в основном получают из минералов гематита и магнетита. В меньшей степени он также может быть получен из минералов таконита, лимонита и сидерита. У него есть четыре различные аллотропные формы, а это означает, что у него четыре различные структурные формы, в которых атомы связываются по-разному. Они называются ферритами, известными как альфа (магнитная), бета, гамма и омега.
Роль в жизни человека
Химический элемент железо является важным питательным веществом в нашем рационе. Его дефицит, один из наиболее распространенных недостатков питательных веществ, может вызвать анемию и усталость, которые влияют на способность выполнять физическую работу у взрослых. Это также может привести к ухудшению памяти и других психических функций у подростков.
Есть два типа пищевого железа: гемовое и негемовое. Гемовое является наиболее легко усваиваемым типом, содержится в мясе, рыбе и птице, тогда как второй тип, который также усваивается, но в меньшей степени, содержится в растительных продуктах (таких как шпинат, капуста и брокколи) и мясе. Люди потребляют до 30 процентов гемового железа по сравнению с 2-10 процентами негемового. При этом продукты, богатые витамином С, такие как помидоры или цитрусовые, могут помочь организму усваивать его.

Молярная масса железа
В химии формула веса представляет собой величину, вычисляемую путем умножения атомного веса каждого элемента в химической формуле на количество его атомов с последующим сложением всех этих результатов вместе. Эти параметры используются в разных целях. Например, для объемных стехиометрических расчетов обычно определяют молярную массу железа. Ее также называют стандартной или средней атомной.

Этот параметр имеет свое собственное обозначение. Поиск молярной массы железа начинается с единицы грамм на моль (г/моль). При расчете молекулярного веса химического соединения это указывает на то, сколько граммов содержится в одном моле этого вещества. Фактически она отображает просто вес в атомных единицах всех атомов в данной формуле. Таким образом, она представляет собой среднюю атомную массу железа. Расчет этой формулы особенно полезен при определении относительных весов реагентов и продуктов в химической реакции.
Для того чтобы найти необходимый параметр, достаточно взять Периодическую таблицу, найти в ней Fe. Над ним будет число 26, а внизу - 55,85, это и есть молярная масса железа.
Похожие статьи
- Многочлены. Разложение многочлена на множители: способы, примеры
- Практическое значение биологии в жизни человека, в медицине, в пищевой промышленности
- Теория вероятности: формулы и примеры решения задач
- Белоруссия или Беларусь: как правильно говорить и писать?
- Зачем нужна география в жизни? Зачем нужно изучать географию?
- И. Бунин "Одиночество": анализ стихотворения по плану
- Закрыть гештальт - что это? Значение и особенности
