Ионы – это заряженные атомы и атомные группы. Понятие об ионных реакциях и заряде ионов
Впервые термин "ион" был введен в 1834 году, в чем заслуга Майкла Фарадея. После изучения действия электрического тока на растворы солей, щелочей и кислот он пришел к выводу, что в них содержатся частицы, имеющие некий заряд. Катионами Фарадей назвал ионы, которые в электрическом поле двигались к катоду, имеющему отрицательный заряд. Анионы - отрицательно заряженные неэлементарные ионные частицы, которые в электрическом поле движутся к плюсу - аноду.
Данная терминология применяется и сейчас, а частицы изучаются далее, что позволяет рассматривать химическую реакцию как результат электростатического взаимодействия. Многие реакции протекают по этому принципу, что позволило понять их ход и подобрать катализаторы и ингибиторы для ускорения их протекания и для угнетения синтеза. Также стало известно, что многие вещества, особенно в растворах, всегда находятся в виде ионов.
Номенклатура и классификация ионов
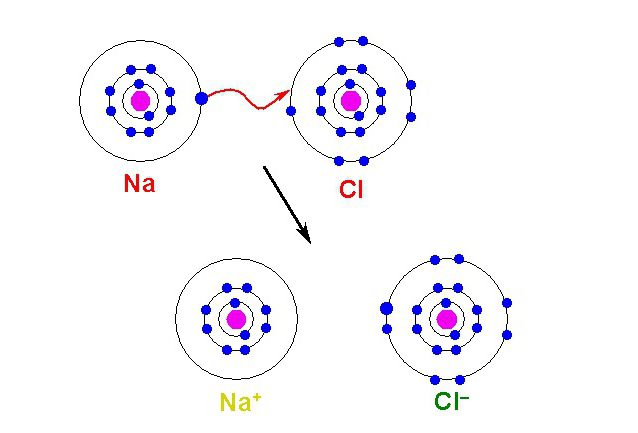
Ионы - это заряженные атомы или группа атомов, которая в ходе химической реакции потеряла или приобрела электроны. Они составляют внешние слои атома и могут теряться из-за низкой силы притяжения ядра. Тогда результатом отсоединения электрона является положительный ион. Также если атом имеет сильный ядерный заряд и узкую электронную оболочку, ядро является акцептором дополнительных электронов. В результате этого образуется отрицательная ионная частица.
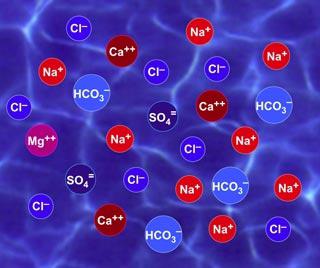
Сами ионы - это не только атомы с избыточной или недостаточной электронной оболочкой. Это может быть и группа атомов. В природе чаще всего существуют именно групповые ионы, которые присутствуют в растворах, биологических жидкостях тел организмов и в морской воде. Имеется огромное количество видов ионов, названия которых вполне традиционны. Катионы - это ионные частицы, заряженные положительно, а заряженные отрицательно ионы - это анионы. В зависимости от состава их называют по-разному. Например, катион натрия, катион цезия и другие. Анионы называются по-другому, так как чаще всего состоят из многих атомов: сульфат-анион, ортофосфат-анион и другие.
Механизм образования ионов
Химические элементы в составе соединений редко являются электрически нейтральными. То есть они почти никогда не находятся в состоянии атомов. В образовании ковалентной связи, которая считается самой распространенной, атомы также имеют некий заряд, а электронная плотность смещается вдоль связей внутри молекулы. Однако заряд иона здесь не формируется, потому как энергия ковалентной связи меньше, нежели энергия ионизации. Потому, несмотря на различную электроотрицательность, одни атомы не могут полностью притянуть электроны внешнего слоя других.
В ионных реакциях, где разница электроотрицательности между атомами достаточно большая, один атом может забирать электроны внешнего слоя у другого атома. Тогда созданная связь сильно поляризуется и разрывается. Затраченная на это энергия, которая создает заряд иона, называется энергией ионизации. Для каждого атома она различная и указывается в стандартных таблицах.
Ионизация возможна только в том случае, когда атом или группа атомов способен либо отдавать электроны, либо акцептировать их. Чаще всего это наблюдается в растворе и кристаллах солей. В кристаллической решетке также присутствуют почти неподвижные заряженные частицы, лишенные кинетической энергии. А поскольку в кристалле нет возможности для передвижения, то реакция ионов протекают чаще всего в растворах.
Ионы в физике и химии
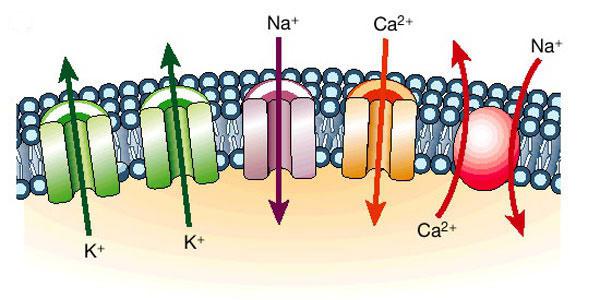
Физики и химики активно изучают ионы по нескольким причинам. Во-первых, эти частицы присутствуют во всех известных агрегатных состояниях вещества. Во-вторых, энергию отрыва электронов от атома можно измерить, чтобы использовать это в практической деятельности. В-третьих, в кристаллах и растворах ионы ведут себя по-разному. И, в-четвертых, ионы позволяют проводить электрический ток, а физико-химические свойства растворов меняются в зависимости от концентраций ионов.
Ионные реакции в растворе
Сами растворы и кристаллы следует рассмотреть детальнее. В кристаллах солей существуют отдельно расположенные положительные ионы, к примеру, катионы натрия и отрицательные, анионы хлора. Структура кристалла удивительна: за счет сил электростатического притяжения и отталкивания ионы ориентируются особым образом. В случае с хлоридом натрия они образуют так называемую алмазную кристаллическую решетку. Здесь каждый натриевый катион окружен 6 хлоридными анионами. В свою очередь, каждый хлоридный анион окружает 6 анионов хлора. Из-за этого простая поваренная соль и в холодной и горячей воде растворяется почти с одинаковой скоростью.

В растворе тоже не существует цельной молекулы хлорида натрия. Каждый из ионов здесь окружается диполями воды и хаотично передвигается в ее толще. Наличие зарядов и электростатических взаимодействий приводит к тому, что солевые растворы воды замерзают при температуре чуть меньше нуля, а кипят при температуре выше 100 градусов. Более того, если в растворе присутствуют другие вещества, способные вступить в химическую связь, то реакция протекает не с участием молекул, а ионов. Это создало учение о стадийности химической реакции.
Те продукты, которые получаются в конце, не образуются сразу в ходе взаимодействия, а постепенно синтезируются из промежуточных продуктов. Изучение ионов позволило понять, что реакция протекает как раз по принципам электростатических взаимодействий. Их результатом является синтез ионов, которые электростатически взаимодействуют с другими ионами, создавая конечный равновесный продукт реакции.
Резюме
Такая частица, как ион, это электрически заряженный атом или группа атомов, которая получается в ходе потери или приобретения электронов. Самым простым ионом является водородный: если он теряет один электрон, то представляет собой лишь ядро с зарядом +1. Он обуславливает кислую среду растворов и сред, что важно для функционирования биологических систем и организмов.
Ионы могут иметь как положительные, так и отрицательные заряды. За счет этого в растворах каждая частица вступает в электростатическое взаимодействие с диполями воды, что также создает условия для жизни и передачи сигналов клетками. Более того, в ионные технологии развиваются дальше. К примеру, созданы ионные двигатели, которыми оснащалось уже 7 космических миссий NASA.
Похожие статьи
- Серебряная вода: польза и вред, свойства, применение, отзывы
- Что такое ионизация: определение, функции, методы и особенности
- Ионизатор воздуха: что это такое? Инструкция, принцип работы, польза и вред
- Окислительно-восстановительный потенциал: расчет и измерение
- Ионная связь: примеры соединений
- Основные законы химии. Основные понятия и законы химии
- Литий - что это такое? Атом, ядро, энергия лития. Литий-ионные аккумуляторы
