Первый закон термодинамики для обычного человека
Вся деятельность человека основывается на потреблении энергии. Без энергии сложно представить себе активность организма, функционирование всех благ для людей. Она важна как внутри человека, так и для его внешнего существования. Различные отрасли производства не могут сами по себе работать, ведь они требуют энергии. Перевозка товаров, отопление помещений, синтез новых веществ в клетках организма - все это происходит благодаря способности производить работу.
Место энергии в термодинамике
Для того чтобы определить, какое место занимает энергия в этой отрасли науки, следует узнать, что конкретно подразумевает термин "термодинамика". Это область физики, в которой углубленно изучаются процессы превращения энергии. Всем известен тот факт, что энергия представлена в нескольких формах: она может быть химической, электрической, тепловой, механической и световой. В данной отрасли науки даже есть свои законы и принципы, например первый закон термодинамики, а также некоторые другие. Исходя из этого, можно сказать, что не существовало бы этой области знаний, если бы не было известно свойств вышеописанной физической величины.
Каким образом происходит превращение энергии?

Многим непонятен факт перехода энергии из одного состояния в другое. Но мы в повседневной жизни настолько часто пользуемся переходящей энергией, что уже не отдаем отчета себе в том, откуда она берется. Так, например, ежедневно садясь в автомобиль, мы не думаем о том, что в момент езды химическая энергия переходит в электрическую. В электромоторе начальная электрическая энергия переходит в механическую, а в паровой турбине тепло преобразуется в механическую физическую величину. При всем этом есть определенные количественные соотношения разных форм энергии. Но при преобразовании происходят процессы с некоторыми количественными потерями: потребление полезной энергии всегда выше, чем ее вырабатывание. Это явление легко объясняется: преобразование не обходится без трения, во время него часть энергии становится теплом и рассеивается в пространстве. Получается, что эта часть уже не может быть использована как полезная величина. Таким образом, любое преобразование не проходит без потерь.
Первый закон термодинамики
Изучая процесс преобразования энергии, ученые открыли два фундаментальных закона. Эта статья будет посвящена первому из них. Этот закон термодинамики гласит: при любом изменении - химическом или физическом - количество энергии остается постоянным. По-другому, он еще называется законом сохранения энергии. Из этого определения следует, что энергия внезапно не появляется и просто так не исчезает. Если в процессе какой-либо деятельности она переходит в разные формы, из одной в другую, то ее общее количество не меняется. Иными словами, энергия не создается и не уничтожается, что отображает первый закон термодинамики. Определение в разных источниках может изменяться, но суть остается неизменной.

История открытия этого закона
Начало свое закон берет еще с середины XIX века. Немецкий врач Майер, наблюдая за тем, как в тропиках изменяется цвет крови человека, задумался о взаимосвязи таких физических понятий, как тепло и энергия. В свою очередь, известный ученый Джоуль обратил внимание на разработки Майера, что-то дополнил со своей стороны. Все данные по этому закону объединил еще один немецкий врач, Гельмгольц, когда изучал физические основы органов восприятия - слуха и зрения человека. Именно он сформулировал закон в таком виде, каким его на сегодняшний день знает весь мир.
Типы обмена энергии
Теплота, которая возникает при переходе одного вида энергии в другой, влияет на изменение внутренней энергии предмета. Когда она меняется, появляется противодействие работе внешних сил, которые влияют на этот предмет. Внутренняя энергия может быть кинетической (это движение атомов предмета), потенциальной (она хранится в химических связях между атомами), гравитационной энергией всей системы (т. е. влияние на предмет гравитационных сил, которые проявляются и внутри). Исходя из этих видов, ученые выделили определенные типы обмена энергии.
- Под первым из них принято понимать предизолированные системы - здесь отсутствует обмен энергией и другими элементами определенной системы.
- Второй тип - закрытые системы, характеризуется отсутствием обмена элементов систем, но в незначительной степени происходит обмен энергией.
- Открытые системы (третий тип обмена) характеризуются обменом и энергией, и их элементами.
Понятие внутренней энергии в термодинамике
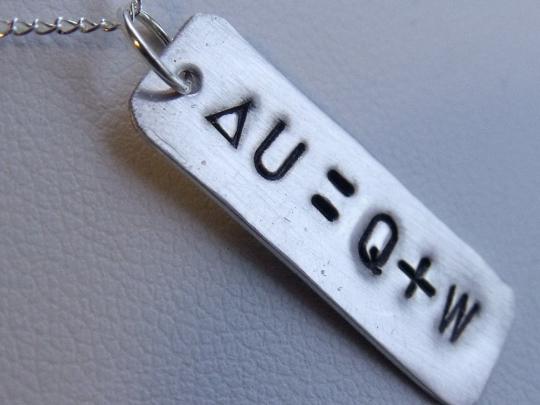
Внутренняя энергия предмета или системы в термодинамике играет почти ключевую роль. На самом деле это сложное объединение нескольких потоков активности молекул и атомов. Она слагается из таких видов, как энергия вращательного и поступательного движения молекул, энергия движений атомов и групп атомов, которая находится внутри молекул и излучается при колебании этих частиц. Еще к внутренней энергии предмета относят ядерную энергию атомов и энергию взаимодействия между собой молекул. Uвн зависит от начального состояния предмета и конечных показателей его состояния. Эта энергия непрерывна, как и обозначает ее первый закон термодинамики. Ее можно легко рассчитать по следующей формуле: тепло, добавленное системе, минус совершенная этой системой работа. Здесь речь идет не о характере процесса изменения внутренней энергии, даже не о конечном состоянии равновесия, так как это определяет уже второй закон термодинамики.
Взаимосвязь тепла и внутренней энергии
Эти понятия очень тесно связаны между собой. Допускается, что тепло является частью внутренней энергии системы. Разберемся, что же собой представляет тепло. Сам предмет не обладает таковым в обычном понимании этого слова. Можно сказать, что тепло - это энергия, которая переходит от объекта, имеющего высокую температуру, к объекту с температурой меньшей, чем у первого.

Иначе говоря, это часть внутренней энергии предмета, которая переносится от него, так как он имеет показатели температуры выше. Такой перенос в физике и химии называется нагревом.
Первый закон термодинамики, химия
Этот закон имеет фундаментальное значение не только для физических опытов, изучения явлений и открытия протекания новых процессов, но и для другой науки - химии - и смежных ее отраслей. При изучении существования и перехода энергии в разные формы в ракурсе химических реакций организма или предмета открывается горизонт интересных исследований и закономерностей в плоскости биоэнергетики.

У многих может возникнуть ощущение, что первый закон термодинамики отдален от жизни обычного человека, что молекулы и атомы для понимания подвластны только малому количеству посвященных людей. Но это далеко не так. В основе жизни каждого живого организма лежит обмен веществ, который не может происходить без превращения энергии. Поэтому особый интерес не только для ученых-физиков, но и для врачей-диетологов, спортивных инструкторов представляют химические процессы превращения энергии в организме человека. Ведь зная все особенности этого процесса, можно успешно помогать людям избавляться от лишних килограммов, а также следить за собой с помощью правильно составленного меню, состоящего из здоровой пищи.
Похожие статьи
- Законы термодинамики и их описание
- Второй закон термодинамики. Трактовки, теоретическое и практическое обоснование
- Основные законы химии. Основные понятия и законы химии
- Механическая энергия. Закон сохранения механической энергии. Применение закона
- Что такое базальная температура? Женское здоровье
- Высокое нижнее давление: о чем это говорит?
- "Детство" Льва Николаевича Толстого. Краткое содержание произведения
