Получение спиртов, применение, свойства. Способы получения спиртов
Спирты распространены в природе. Большинство людей знакомы с этиловым спиртом (этанолом) - активным ингредиентом алкогольных напитков, но он является лишь одним из семейства органических соединений, известных как спирты. Получение их, прежде всего этилового (винного в результате ферментативного брожения виноградного сока стало одним из первых химических техпроцессов, освоенных человечеством.
Номенклатура спиртов
Спирты представляет собой органические соединения гидроксильной (ОН) функциональной группы с алифатическим атомом углерода. Поскольку ОН является принадлежностью молекул всех спиртов, их часто представляют как производными воды с общей формулой ROH, где R обозначает алкильную группу.
Получение спиртов метанола (СН3ОН) и этанола (СН3СН2ОН), являющихся первыми двумя членами их гомологического ряда, является важной задачей химической промышленности многих стран. При содержании от одного до четырех атомов углерода их часто называют общими именами, в которых за названием алкильной группы следует слово спирт:
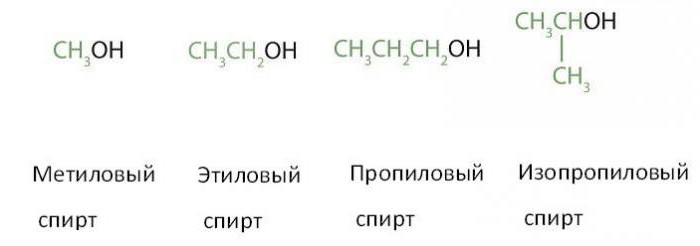
Можно видеть, что все четыре (две последние являются изомерами одного вещества) представленные выше молекулы спиртов содержат одну гидроксильную группу. По этому признаку все они относятся к классу одноатомных спиртов (бывают и двух-, трех, четырех- и многоатомные). Кроме того, все они являются производными предельных углеводородов из ряда алканов: метана, этана, пропана (названия спиртов получают добавлением к названию алкена окончания «-ол»). Поэтому их еще называют предельными одноатомными спиртами.
Одноатомные спирты
Получение, свойства (как физические, так и химические) этих соединений зависят от количества атомов углерода, присоединенных к его же атому, непосредственно связанному с группой ОН. Поэтому одноатомные спирты могут быть сгруппированы в три класса на этой основе.
- Первичные спирты имеют молекулу, в которой один атом углерода, связанный с ОН-группой, присоединен к еще одному атому C. Их общая формула RCH2ОН. Например, этанол – первичный спирт.
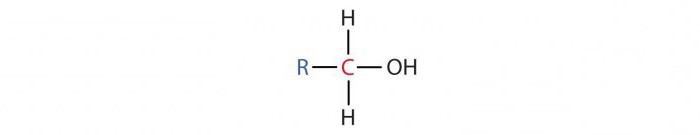
- Вторичные спирты имеют в молекуле один атом углерода с ОН-группой, присоединенный к двум другими атомам C. Их общая формула R2СНОН. К ним относятся пропиловый и изопропиловый спирты.
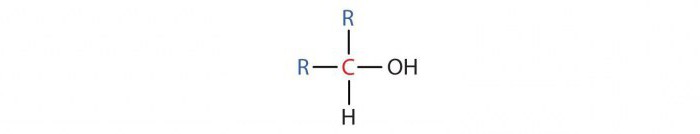
- Третичные спирты содержат в молекуле атом углерода с ОН-группой, присоединенный к трем другими атомам C. Их общая формула R3СОН.

Получение одноатомных спиртов в промышленности возможно целым рядом способов, которые будут рассмотрены ниже.
Метанол как продукт природного газа
Метанол получают смешиванием газа водорода и монооксида углерода при высоких температурах и давлениях (200 ат, 350 °C) в присутствии катализатора, состоящего из оксида цинка (ZnO) и оксида хрома (Cr2 O3) в качестве катализатора: 2H2 + CO → CH3OH.

При этом сырьем для получения реагентов являются природный газ и водяной пар, смешивая которые, получают синтез – газ, представляющий собой смесь CO и H2.
Метанол является важным растворителем и используется в качестве автомобильного топлива, либо в виде чистой жидкости – в некоторых гоночных автомобилях, либо в качестве высокооктановой добавки в бензин. Получение и применение спиртов в мире, и в частности метанола, измеряется миллионами тонн. По итогам 2013 г. в мире было потреблено 66 млн т метанола, из них 65 % в Азии, 17 % - в Европе и 11 % - в США.
Получение предельных спиртов из алкенов
Многие простые весовые спирты, имеющие промышленное значение, производятся гидратацией (добавлением воды) алкенов (этилена, пропилена, бутена). Этанол, изопропанол, бутанол (вторичный и третичный) получают по этой реакции.
Известны прямой и косвенный способы получения спиртов гидратацией. Прямой позволяет избежать образования стабильных промежуточных продуктов, как правило, с помощью кислых катализаторов.
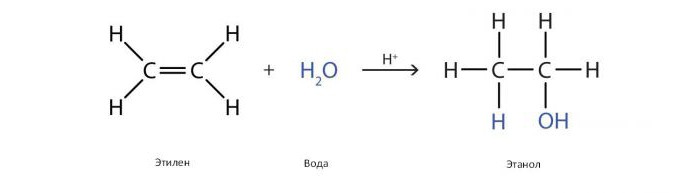
Катализатором обычно является фосфорная кислота, адсорбированная на пористом носителе, таком как силикагель или кизельгур. Этот катализатор был впервые использован для крупномасштабного производства этанола в США компанией "Шелл" в 1947 году. Реакцию проводят в присутствии пара высокого давления при 300 °C, причем между этиленом и паром поддерживается соотношение 1,0: 0,6.
Аналогичная реакция производства изопропилового спирта с катализаторов в виде серной кислоты выглядит следующим образом
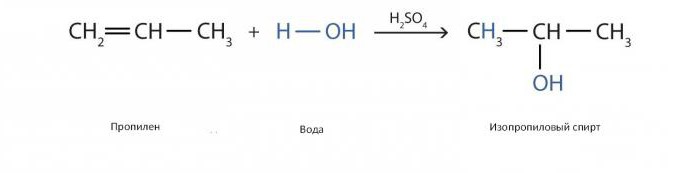
Косвенный способ гидратации этилена
В косвенным способе, на практике впервые примененном в промышленном масштабе в 1930 году, но сегодня считающимся почти полностью устаревшим, реакция получения спиртов заключается в превращении алкена в сульфат эфиры, который затем гидролизуют. Традиционно алкен обрабатывают серной кислотой с получением алкильные сульфатных эфиров. В случае производства этанола, этот шаг может быть записан так: Н2SO4 + С2 Н4 → C2H5 -O-SO3H
Впоследствии этот сульфат эфира гидролизуют до регенерации серной кислоты и освобождения этанола: С2Н5-O-SO3H + H2O → H2SO4 + С2Н5ОН.
Способы получения спиртов чрезвычайно разнообразны, но нижеописанный процесс, пожалуй, известен, хотя бы понаслышке каждому читателю.
Спиртовое брожение
Это биологический процесс, в котором молекулы, такие как глюкоза, фруктоза и сахароза, преобразуются в клеточную энергию с параллельным производством этанола и углекислого газа в качестве продуктов метаболизма. Брожение катализируется ферментами, содержащимися в дрожжах и протекает по сложному многоступенчатому механизму, которое включает в общем случае преобразование (на первом этапе) крахмала, содержащегося в растительных зернах, в глюкозу с последующим получением из нее этанола. Поскольку дрожжи выполняют это преобразование в отсутствие кислорода, спиртовое брожение считается анаэробным процессом.
Реакции получения спиртов брожением можно представить следующим образом:
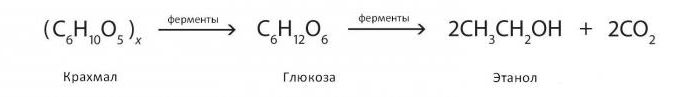
Способы получения алкогольных напитков
Весь этанол, содержащийся в алкогольных напитках производится посредством ферментации, вызванной дрожжами.
Вино производится путем ферментации из натуральных сахаров, присутствующих в винограде; сидр получают аналогичной ферментацией природного сахара в яблоках и грушах, соответственно; и другие фруктовые вина производятся ферментацией сахаров в любых других видах фруктов. Бренди и коньячные спирты (например, сливовица) производятся при перегонке напитков, получаемых брожением фруктовых сахаров.
Медовые напитки производятся путем ферментации из натуральных сахаров, присутствующих в меде.
Пиво, виски, и водка производятся путем ферментации зерен крахмала, которые преобразуются в сахар под действием фермента амилазы, присутствующей в зерновых ядрах, подвергшихся солодовому проращиванию. Другие источники крахмала (например, картофель и не солодовое зерно) могут быть добавлены к смеси, так как амилаза будет действовать также и на их крахмал.
Рисовые вина (в том числе саке) получают путем брожения зерновых крахмалов, превращаемых в сахар грибками Aspergillus огугае.
Ром и некоторые другие напитки получают ферментацией и дистилляцией сахарного тростника. Ром, как правило, производится из продукта сахарного тростника – патоки.
Во всех случаях брожение должно происходить в сосуде, который позволяет двуокиси углерода выходить, но предотвращает приход наружного воздуха. Это нужно потому, что воздействие кислорода предотвращает образование этанола, а накопление диоксида углерода создает риск разрыва сосуда .

Реакция нуклеофильного замещения
Получение спиртов в лабораториях производится способами, которые используют в качестве исходных продуктов для реакций химические вещества самых разнообразных классов, от углеводородов до карбонильных соединений. Существует несколько способов, которые сводятся к нескольким основным реакциям.
Первичные галогеналканы реагируют с водными растворами щелочей NaOH или КОН, образуя, образуя, главным образом, первичные спирты в реакции нуклеофильного алифатического замещения. Когда, например, метилбромид реагирует с раствором едкого натра, то гидроксильные группы, образующинся при диссоциации щелочи, замещают ионы брома с образованием метанола.
Несколько реакций, позволяющих выполнять получение спиртов в лабораториях, приведены ниже.
Нуклеофильное присоединение.
Реактивы Гриньяра (соединения магния с алкилгалогенидами – иодидами или бромидами), а также металлоорганические соединения меди и лития реагируют с карбонильными группами (C=O) альдегидов с образованием первичных и вторичных спиртов в зависимости от механизма присоединения.Аналогичные реакции с кетонами приводят к третичным спиртам.
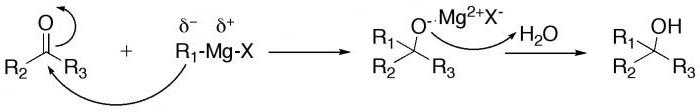
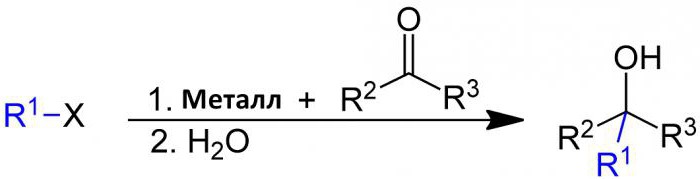
Реакция Барбье протекает между галогеналканом и карбонильной группой в качестве электрофильного субстрата в присутствии магния, алюминия, цинка, индия, олова или его солей. Продуктом реакции является первичный, вторичный или третичный спирт. Механизм ее протекания аналогичен реакции Гриньяра с той разницей, что реакция Барбье является синтезом в одном сосуде, тогда как реактив Гриньяра получают отдельно перед добавлением карбонильного соединения.
Реакция восстановления
Альдегиды или кетоны восстанавливаются до спиртов с боргидридом натрия (NaBH4) или (после кислотной обработки) с литийалюминий гидридом (LiAlH).
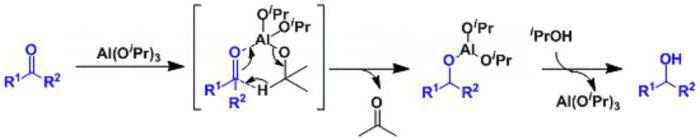
В реакции Меервейна-Пондорфа-Верли (MPV) получение спиртов путем восстановления их из кетонов и альдегидов происходит с использованием алюминиевого алкоксидного катализатора. Достоинства MPV заключаются в ее высокой хемоселективности и использовании дешевого, экологически чистого металлического катализатора. Реакция была обнаружена Меервейном и Шмидтом, и независимо Верли в 1925 г. Они обнаружили, что смесь алюминиевого этоксида и этанола может восстановить альдегиды до их спиртов. Понндорф применил реакцию к кетонам и обновил катализатор до изопропилата алюминия (Al(O-i-Pr)3, где i-Pr означает изопропиловую группу (CH(CH3)2). в целях получения изопропанола.
Общее уравнение получения спирта путем MPV-восстановления кетонов до спиртов выглядит так:
Это, конечно, не все, что можно сказать относительно спиртов и их свойств, но общее представление о них, надеемся, вам составить удалось.
Похожие статьи
- Виды спирта для производства водки
- Спирт "Люкс" и "Альфа": что лучше, в чем разница. Классификация спиртов
- Глицерин: свойства и применение
- Одноатомные спирты. Как получить предельный одноатомный спирт
- Как правильно развести спирт для внутреннего потребления
- Какой спирт можно пить без угрозы здоровью? Можно ли пить медицинский спирт
- Этиловый спирт. Спирт этиловый медицинский - применение


