Одноатомные спирты. Как получить предельный одноатомный спирт
Органические кислородсодержащие соединения, одними из которых являются различные спирты, являются важными функциональными производными углеводородов. Они бывают одноатомными, двух- и многоатомными. Одноатомные спирты - это, по сути, производные углеводородов, в молекулярной составляющей которых - одна гидроксильная группа (обозначаемая «-OH»), связанная с насыщенными атомами углерода.

Распространение
Одноатомные спирты достаточно широко распространены в природе. Так, метиловый спирт в небольших количествах содержится в соке ряда растений (например, борщевик). Этиловый спирт, являясь продуктом спиртового брожения органических соединений, содержится в подкисших фруктах и ягодах. Цетиловый спирт найден в китовом жире. Пчелиный воск включает цериловый, мирициловый спирты. В лепестках роз обнаружен 2-фенилэтанол. Терпеновые спирты в виде душистых веществ представлены во многих пряно-ароматических культурах.
Классификация
Спирты подразделяют по молекулярному числу гидроксильных групп. Прежде всего на:
- одноатомные спирты (к примеру, этанол);
- двухатомные (этандиол);
- многоатомные (глицерин).
По природе углеводородного радикала спирты подразделяются на ароматические, алифатические, циклические. В зависимости от типа атома углерода, имеющего связь с гидроксильной группой, спирты рассматривают как первичные, вторичные и третичные. Общая формула одноатомного спирта в применении к предельным одноатомным спиртам выражается значением: СnH2n+2O.
Номенклатура
Название спиртов по радикально-функциональной номенклатуре образуется из названия, ассоциируемого с гидроксильной группой радикала, и слова «спирт». По систематической номенклатуре IUPAC название спирта образуется от соответствующего алкана с добавлением окончания «-ол». Например:
- метанол – метиловый спирт;
- метилпропанол-1-2 – изобутиловый (третбутиловый);
- этанол – этиловый;
- бутанол-1-2 – бутиловый (вторбутиловый);
- пропанол-1-2 – пропиловый (изопрапиловый).
Нумерация по правилам IUPAC классифицируется положением гидроксильной группы, она получает меньший номер. Например: пентандиол-2-4, 4-метилпентанол-2 и т.д.
Изомерия
Предельные одноатомные спирты обладают следующими типами структурной и пространственной изомерии. Например:
- Углеродного скелета.
- Изомерные простым эфирам.
- Положения функциональной группы.
Пространственная изомерия спиртов представлена оптической изомерией. Оптическая изомерия возможна при наличии в молекуле асимметрического атома углерода (содержащего четыре разных заместителя).
Способы получения одноатомных спиртов
Получить предельный одноатомный спирт можно несколькими методами:
- Гидролизом галогеналканов.
- Гидратацией алкенов.
- Восстановлением альдегидов и кетонов.
- Магнийорганическим синтезом.
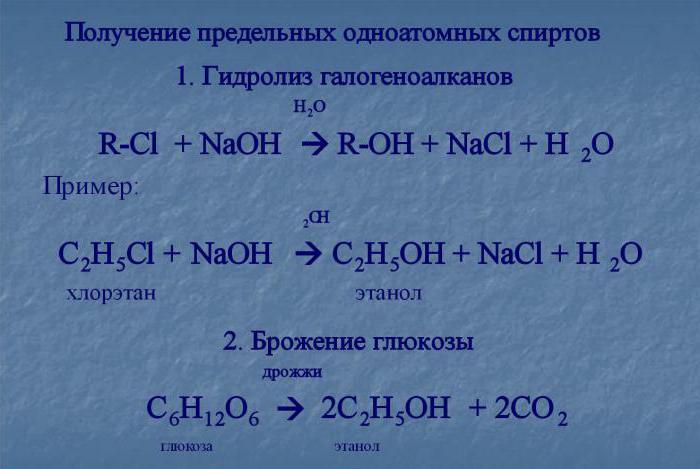
Гидролиз галогеналканов – это один из распространенных лабораторных способов получения спиртов. Обработкой водой (как альтернатива – водным раствором щелочи) спирты получают первичные и вторичные:
CH3 - CH2 -Br + NaOH → CH3 - CH2 - OH + NaBr.
Третичные галогеноалканы гидролизуются еще легче, однако у них легче протекает побочная реакция элиминирования. Поэтому третичные спирты получают другими методами.
Гидратация алкенов производится присоединением к алкенам воды в присутствии кислотосодержащих катализаторов (H3PO4). Метод лежит в основе промышленного получения таких спиртов, как этиловый, изопропиловый, трет-бутиловый.
Восстановление карбонильной группы осуществляют водородом в присутствии катализатора гидрирования (Ni или Pt). Из кетонов при этом образуются вторичные спирты, из альдегидов – первичные предельные одноатомные спирты. Формула процесса:
CH3 - C = O (-H) + H2 (этаналь) → CH3 - CH2 - OH (этанол).
Присоединением к альдегидам и кетонам алкилмагнийгалогенидов получают магний-органические соединения. Реакцию проводят в сухом диэтиловом эфире. Последующий гидролиз магнийорганических соединений образует одноатомные спирты.
Первичные спирты образуются по реакции Гриньяра только из формальдегида и любых алкилмагнийгалогенидов. Другие альдегиды дают по этой реакции вторичные спирты, кетоны – третичные спирты.
Промышленный синтез метанола
Промышленные методы, как правило, являются непрерывными процессами с многократной рециркуляцией больших масс реагирующих веществ, осуществляемые в газовой фазе. Промышленно важными спиртами являются метанол и этанол.
Метанол (его объемы производства самые большие среди спиртов) до 1923 года получали сухой перегонкой (нагреванием без доступа воздуха) древесины. Сегодня его генерируют из синтез-газа (смеси CO и H2). Процесс проводят под давлением 5-10 МПа с использованием оксидных катализаторов (ZnO + Cr2O3, CuO + ZnO + Al2O3 и других) в интервале температур 250-400˚С, в результате получали предельные одноатомные спирты. Формула реакции: CO + 2H2 → CH3OH.
В 80-е годы при изучении механизма этого процесса было установлено, что метанол образуется не из угарного газа, а из углекислого газа, получающегося при взаимодействии угарного газа со следами воды.
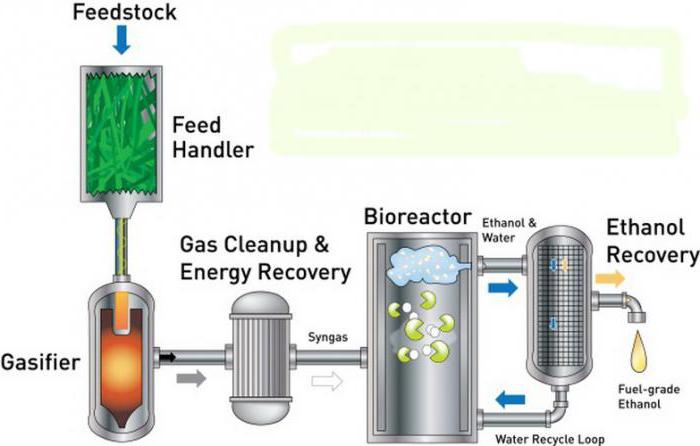
Промышленный синтез этанола
Распространенным производственным методом синтеза технического этанола является гидратация этилена. Формула одноатомного спирта этанола получит следующий вид:
CH2 = CH2 + H2O → CH3 - CH2OH.
Процесс проводят под давлением 6-7 МПа в газовой фазе, пропуская этилен и пары воды над катализатором. Катализатором выступают фосфорная либо серная кислоты, нанесенные на силикагель.
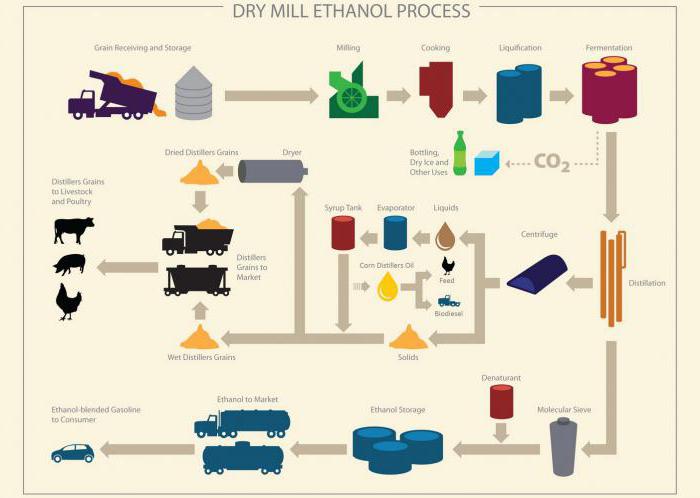
Пищевой и медицинский этиловый спирт получают ферментативным гидролизом сахаров, содержащихся в винограде, ягодах, злаках, картофеле с последующим сбраживанием образующейся глюкозы. Брожение сахаристых веществ вызывается дрожжевыми грибками, относящимися к группе ферментов. Для процесса наиболее благоприятна температура 25-30˚С. На промпредприятиях применяют этанол, полученный сбраживанием образующихся при гидролизе древесины и отходов целлюлозно-бумажного производства углеводов.
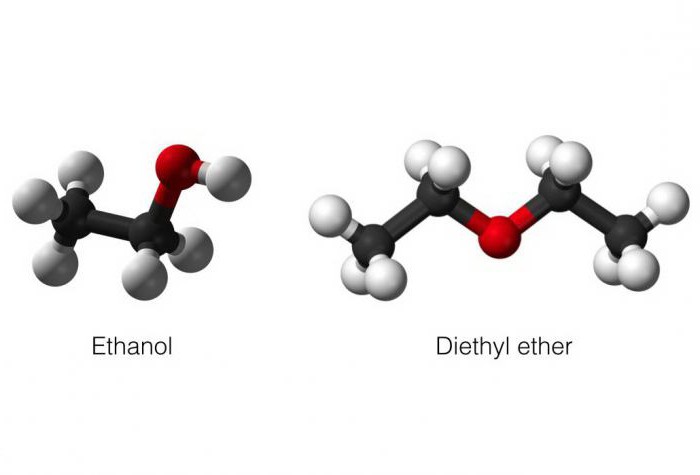
Физические свойства одноатомных спиртов
В молекулах спиртов существуют атомы водорода, связанные с электроотрицательным элементом – кислородом, практически лишенные электронов. Между этими атомами водорода и атомами кислорода, имеющими неподеленные пары электронов, образуются межмолекулярные водородные связи.
Водородная связь обусловлена специфическими особенностями атома водорода:
- При оттягивании связывающих электронов к более электроотрицательному атому ядро атома водорода «оголяется», и образуется неэкранированный другими электронами протон. При ионизации любого другого атома все равно остается электронная оболочка, экранирующая ядро.
- Атом водорода имеет малый размер по сравнению с прочими атомами, вследствие чего он способен достаточно глубоко внедряться в электронную оболочку соседнего отрицательно поляризованного атома, не соединяясь с ним ковалентной связью.
Водородная связь примерно в 10 раз слабее обычной ковалентной. Энергия водородной связи находится в пределах 4-60 кДж/моль, для молекул спиртов она составляет 25 кДж/моль. От обычных s-связей она отличается и большей длиной (0,166 нм) по сравнению с длиной связи O-H (0,107 нм).
Химические свойства
Химические реакции одноатомных спиртов определяются наличием в их молекулах гидроксильной группы, являющейся функциональной. Атом кислорода находится в sp3-гибридном состоянии. Валентный угол близок к тетраэдрическому. Две sp3-гибридные орбитали идут на образование связей с другими атомами, а на двух других орбиталях находятся неподеленные пары электронов. Соответственно, на атоме кислорода сосредоточен частичный отрицательный заряд, а на атомах водорода и углерода – частичные положительные заряды.
Связи C-O и C-H – ковалентные полярные (последняя более полярная). Гетеролитический разрыв связи O-H с образованием H+ обусловливает кислотные свойства одноатомных спиртов. Атом углерода с частичным положительным зарядом может быть объектом атаки нуклеофильного реагента.

Кислотные свойства
Спирты являются очень слабыми кислотами, более слабыми, чем вода, но более сильными, чем ацетилен. Они не вызывают изменения окраски индикатора. Окисление одноатомных спиртов проявляется при взаимодействии с активными металлами (щелочными и щелочно-земельными) с выделением водорода и образованием алкоголятов:
2ROH + 2Na → 2RONa + H2.
Алкоголяты щелочных металлов – вещества с ионной связью между кислородом и натрием, в растворе одноатомного спирта они диссоциируют с образованием алкосид-ионов:
CH3ONa → CH3O- + Na+ (метоксид-ион).
Образование алкоголятов возможно также осуществить по реакции спирта с амидом натрия:
C2H5OH + NaNH2 → C2H5ONa + NH3.
А произойдет ли реакция этанола со щелочью? Практически нет. Вода – более сильная кислота, чем этиловый спирт, поэтому здесь устанавливается равновесие. С увеличением длины углеводородного радикала в молекуле спирта кислотные свойства снижаются. Также предельные одноатомные спирты характеризуются снижением кислотности в ряду: первичный → вторичный → третичный.
Реакция нуклеофильного замещения
В спиртах связь C-O поляризована, на атоме углерода сконцентрирован частичный положительный заряд. Как следствие – атом углерода атакуется нуклеофильными частицами. В процессе разрыва связи C-O происходит замещение другим нуклеофилом гидроксильной группы.
Одной из таких реакций является взаимодействие спиртов с галогенводородами или их концентрированными растворами. Уравнение реакции:
C2H5OH + HBr → C2H5Br + H2O.
Для облегчения отщепления гидроксильной группы используют в качестве катализатора концентрированную серную кислоту. Она протонирует атом кислорода, тем самым активируя молекулу одноатомного спирта.
Первичные спирты, как и первичные галогеноалканы, вступают в реакции обмена по механизму SN2. Вторичные одноатомные спирты, как и вторичные галогеноалканы, реагируют с галогеноводородными кислотами. Условия взаимодействия спиртов подчинены природе реагирующих компонентов. Реакционная способность спиртов подчиняется следующей закономерности:
R3COH → R2CHOH → RCH2OH.
Окисление
В мягких условиях (нейтральные или щелочные растворы перманганата калия, хромовой смеси при температуре 40-50°С) окисляются первичные спирты до альдегидов, при нагревании до более высокой температуры – до кислот. Вторичные спирты проходят процесс окисления до кетонов. Третичные окисляются в присутствии кислоты в очень жестких условиях (например, хромовой смесью при температуре 180°С). Реакция окисления третичных спиртов идет через дегидратацию спирта с образованием алкена и окислением последнего с разрывом двойной связи.
Похожие статьи
- Спирт "Люкс" и "Альфа": что лучше, в чем разница. Классификация спиртов
- Получение спиртов, применение, свойства. Способы получения спиртов
- Химические свойства спиртов одноатомных и многоатомных
- Симптомы отравления метиловым спиртом: описание и особенности лечения
- Метиловый спирт: свойства, получение и применение
- Виды спирта для производства водки
- Альдегиды и кетоны. Формула, получение, применение
