Относительная атомная масса элемента в химии и история её определения
В процессе развития науки химия столкнулась с проблемой подсчёта количества вещества для проведения реакций и полученных в их ходе веществ.
На сегодня для подобных расчётов химической реакции между веществами и смесями используют значение относительной атомной массы, внесённой в периодическую таблицу химических элементов Д. И. Менделеева.
Химические процессы и влияние доли элемента в веществах на ход реакции
Современная наука под определением «относительная атомная масса химического элемента» подразумевает, во сколько раз масса атома данного химического элемента больше одной двенадцатой части атома углерода.
С зарождением эры химии потребность в точных определениях хода химической реакции и её результатов росла.
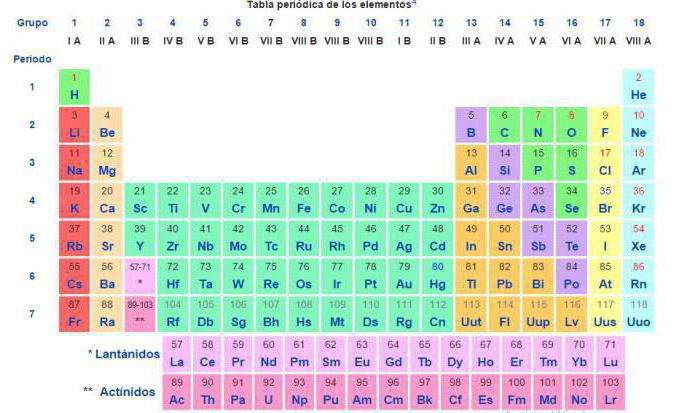
Исторический ход подсчёта вещества
Изначально использовался водород, затем кислород. Но этот способ расчёта оказался неточным. Причиной тому послужило наличие в кислороде изотопов с массой 17 и 18.

Дальтон заложил основы относительной атомной массы элемента
Лишь спустя некоторое время, в 19-м веке, Дальтон предложил вести расчёт по самому лёгкому химическому элементу – водороду. На лекциях своим студентам он демонстрировал на вырезанных из дерева фигурках, как соединяются атомы. По другим элементам он использовал данные, ранее полученные другими учёными.
По экспериментам Лавуазье в воде содержится пятнадцать процентов водорода и восемьдесят пять процентов кислорода. Имея эти данные, Дальтон рассчитал, что относительная атомная масса элемента, входящего в состав воды, в данном случае кислорода, составляет 5,67. Ошибочность его расчётов связана с тем, что он считал неверно относительно количества атомов водорода в молекуле воды.
По его мнению, на один атом кислорода приходился один атом водорода. Воспользовавшись данными химика Остина о том, что в составе аммиака 20 процентов водорода и 80 процентов азота, он рассчитал, чему равна относительная атомная масса азота. Имея этот результат, он пришёл к интересному выводу. Получалось, что относительная атомная масса (формула аммиака ошибочно была принята с одной молекулой водорода и азота) составляет четыре. В своих расчетах ученый опирался на периодическую систему Менделеева. По анализу он рассчитал, что относительная атомная масса углерода - 4,4, вместо принятых до этого двенадцати.

Изотопная составляющая вещества влияет на значение точности относительного атомного веса
При рассмотрении атомных масс элементов можно заметить, что точность по каждому элементу разная. К примеру, по литию она четырёхзначная, а по фтору - восьмизначная.
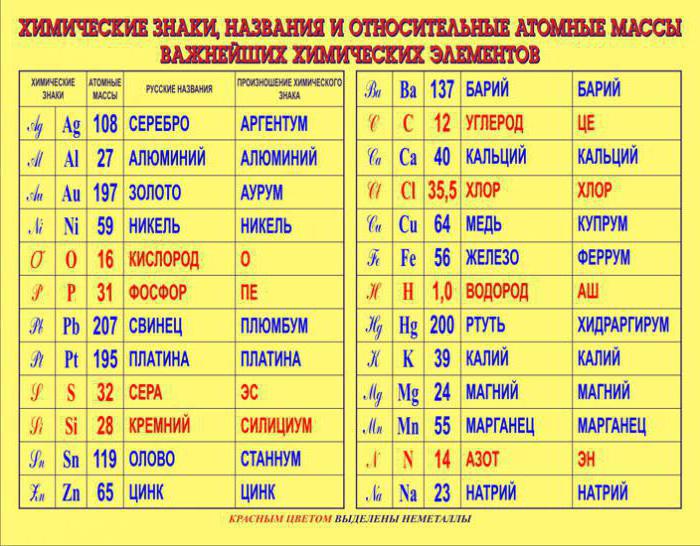
Относительная атомная масса изотопов водорода составляет соответственно два и три. «Тяжёлая» вода (образованная дейтерием и тритием) испаряется хуже. Поэтому в парообразном состоянии изотопов воды меньше, чем в жидком состоянии.
Избирательность живых организмов к различным изотопам
Живые организмы обладают селективным свойством по отношению к углероду. На построение органических молекул используют углерод с относительной атомной массой, равной двенадцати. Поэтому вещества органического происхождения, а также ряд полезных ископаемых, таких как уголь и нефть, содержат меньше изотопной составляющей, чем неорганические материалы.
Микроорганизмы, перерабатывающие и накапливающие серу, оставляют после себя изотоп серы 32. В зонах, где бактерии не перерабатывают, доля изотопа серы - 34, то есть гораздо выше. Именно на основании соотношения серы в породах почвы геологи приходят к выводу о природе происхождения слоя - магматическую природу он имеет или же осадочную.
Из всех химических элементов только один не имеет изотопов - фтор. Поэтому его относительная атомная масса более точная, чем других элементов.
Существование в природе нестабильных веществ
У некоторых элементов относительная масса указана в квадратных скобках. Как видно, это элементы, расположенные после урана. Дело в том, что они не имеют устойчивых изотопов и распадаются с выделением радиоактивного излучения. Поэтому в скобках указан наиболее устойчивый изотоп.
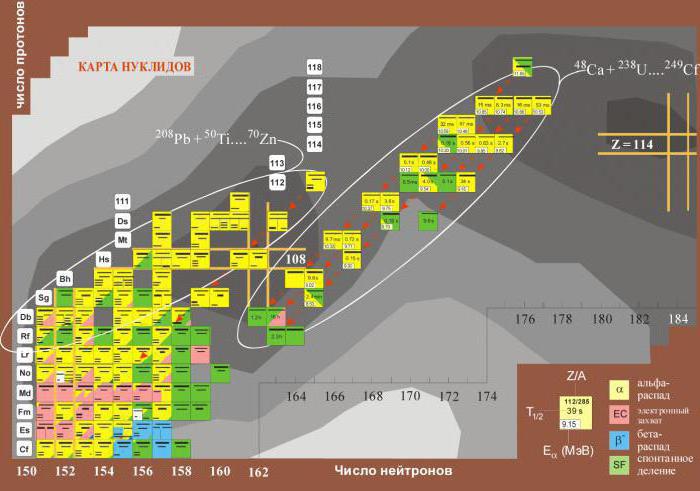
В процессе синтеза новых изотопов и измерения их продолжительности жизни порой удавалось обнаружить нуклиды с продолжительностью полураспада в миллионы раз дольше.
Наука не стоит на месте, постоянно открываются новые элементы, законы, взаимосвязи различных процессов в химии и природе. Поэтому, в каком виде окажется химия и периодическая система химических элементов Менделеева в будущем, лет через сто, - является туманным и неопределённым. Но хочется верить, что накопленные за прошедшие века труды химиков послужат новому, более совершенному знанию наших потомков.
Похожие статьи
- Чему равна молярная масса водорода?
- Что такое число Авогадро?
- Оксид фосфора: получение и взаимодействие
- Молекулярная масса: базовые принципы определения
- Химический элемент - это... Периодическая система химических элементов
- Ванадий: свойства, атомная масса, формула, применение
- Азот - это типичный неметалл
