Углеводороды - это соединения углерода с водородом, не содержащие других элементов. Классификация углеводородов
Что такое углеводороды? Как они классифицируются? Какими особенностями обладают? Попробуем вместе найти ответы на поставленные вопросы.
Углеводороды — это органические соединения, которые в своем составе имеют водород и углерод. Их в органической химии считают базовыми соединениями.
Классификация
В зависимости от состояния связи между углеродами основной цепи, все СхНу принято подразделять на несколько видов. Одинарные соединения углерода с водородом характерны для предельных углеводородов.
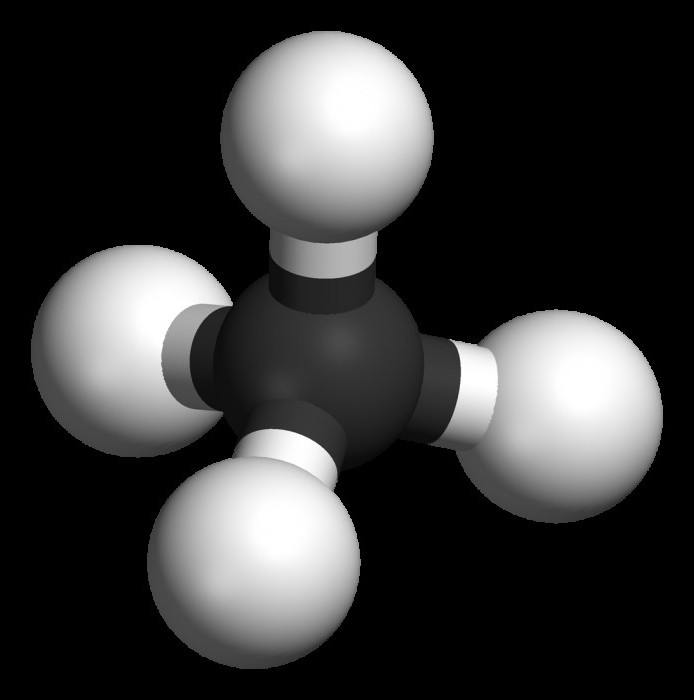
Алканы
Предельные углеводороды — это соединения, имеющие общую формулу СпН2п+2. Среди их особенностей можно упомянуть отсутствие замкнутой структуры, а также одинарные (простые) связи. Их в органической химии называют ациклическими соединениями.
Типичным представителем данного класса является метан – СН4. Именно он начинает гомологический ряд алканов, обладает всеми свойствами, присущими остальным представителям парафинов.
Первые представители данного класса углеводородов являются газообразными веществами, обладающими малой растворимостью в воде, специфическим запахом.
Среди основных химических свойств, которыми обладают представители гомологического ряда алканов, выделим радикальное замещение.
Галогенирование протекает при повышенной температуре либо наличии ультрафиолетового облучения. Реакция протекает в несколько стадий, характеризуется постепенным замещением атомов водорода галогеном. Свойства углеводородов ряда метана объясняются насыщенностью связи между углеродными атомами. Они не способны вступать в реакции присоединения, при этом отлично горят в кислороде воздуха с образованием углекислого газа, водяного пара, выделением достаточного количества тепловой энергии.
Среди основных отраслей применения представителей данного класса углеводородов выделим использование в качестве топлива, а также вариант исходного сырья для производства множества иных органических соединений.
Алкены
Ненасыщенные углеводороды — это соединения, которые имеют одну либо несколько кратных (ненасыщенных) связей между углеродными атомами. Алкены имеют общую формулу СпН2п. Типичным представителем данного класса является этилен.
Эти природные углеводороды входят в состав нефти. Учитывая, что в молекуле содержится двойная связь, для алкенов характерны реакции присоединения. Например, они могут вступать в галогенирование, гидратацию.
Если двойная связь располагается в первом положении, например в бутене-1, присоединение галогеноводорода и гидратация (реакция с водой) протекают по правилу Марковникова. Суть его состоит в том, что при гидрогалогенировании и гидратации водород присоединяется к тому атому углерода, который им максимально насыщен.
Гидроксильная группа или атом галогена присоединяется к атому С, который не насыщен водородом. Качественной реакцией на непредельную (двойную) связь является обесцвечивание бромной воды или перманганата калия.

Циклоалканы
Такие углеводороды — это циклические соединения, являющиеся межклассовыми изомерами для алкенов. Они имеют общую формулу СпН2п, одинарные связи. Учитывая, что данный класс характеризуется замкнутой структурой, они вступают в реакции присоединения, сопровождающиеся разрушением замкнутого цикла, превращением в насыщенные алканы. Основными источниками таких соединений выступают природный и попутный газ, нефть. Несмотря на циклическое строение, в молекулах sp3-гибридизация, валентный угол составляет 109°28'.
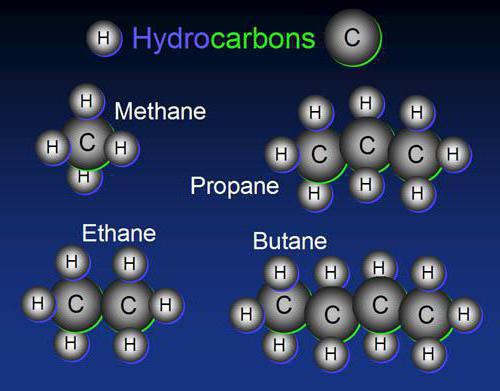
Алкадиены
Чем еще характеризуется органическая химия? Углеводороды этого класса имеют общую формулу СпН2п-2. У всех представителей диеновых углеводородов присутствуют две двойные связи. Ненасыщенность диенов определяет их основные химические свойства. По аналогии с алкенами, диеновые соединения вступают в реакции присоединения.
В качестве тех химических реакций, которые характерны для данных соединений, отметим полимеризацию. Исходным мономером в процессе выступает представитель диенов, а продуктом взаимодействия будет синтетический каучук. При добавлении в получаемый полимер серы, происходит вулканизация, сопровождающаяся образованием резины.
Алкины
Для этих ненасыщенных органических соединений, характеризующихся общей формулой СпН2п-2, можно отметить наличие тройной связи между углеродными атомами. Если она располагается после первого углеродного атома, качественной реакцией на ее присутствие выступает замещение с комплексным соединением серебра.
Так же как и для алкенов, диенов, алкины легко вступают в присоединение по тройной связи. Для них свойственны реакции гидрирования, гидрогалогенирования, галогенирования, гидратации.

Ароматические соединения
Бензол является первым представителем данного класса. Он имеет общую формулу СпН2п-6. В отличие от всех остальных углеводородов, данное соединение имеет ароматическое кольцо. В его образовании принимают участие свободные электроны каждого углеродного атома. Три электрона С образуют гибридные облака, а четвертый электрон не повергается гибридизации. Именно он формирует ароматическое кольцо, которое равномерно распределяется по всей молекуле. Равномерное распределение кольца по структуре объясняет его химическую стабильность. Сам бензол вступает в замещение и присоединение только при жестких условиях.
Толуол, являющийся его гомологом, характеризуется некоторым смещением электронной плотности, поэтому у него выше способность к замещению. Углеводородный радикал является ориентантом 1 рода, входящие заместители (галоген, нитрогруппа) занимают орто-, параположения.
Заключение
Независимо от того, какие особенности структуры имеют различные представители углеводородов, они в своем составе имеют определенное количество атомов углеродов и водородов. Существует определенная тенденция в изменении физических свойств представителей СхНу. Первые представители любого класса имеют газообразное состояние, по мере увеличения относительной молекулярной массы наблюдается планомерный переход в жидкости, затем в твердый вид.
Похожие статьи
- Предельные углеводороды: свойства и применение
- Ароматические углеводороды: все о них
- Органические соединения. Классы органических соединений
- Алканы: общие сведения. Физические и химические свойства алканов
- Химические свойства алкадиенов - непредельных углеводородов
- Химические и физические свойства алкинов
- Органические вещества. Классы органических веществ
