Химические и физические свойства аренов

Существуют органические соединения, молекулы которых содержат небольшое количество атомов водорода, хотя их карбоновый скелет достаточно велик. Такие вещества считаются сильно ненасыщенными, однако, они не вступают в реакции, характерные для алкенов или алкинов. Например, не обесцвечивают растворы перманганата калия или бромной воды. Первыми, полученными химиками из этой группы соединений, оказались вещества, обладающие приятным запахом, поэтому их назвали ароматическими. Существует еще одно название - арены. Номенклатура, изомерия, получение и физические свойства их будут изучены нами в этой статье.

Что такое бензол
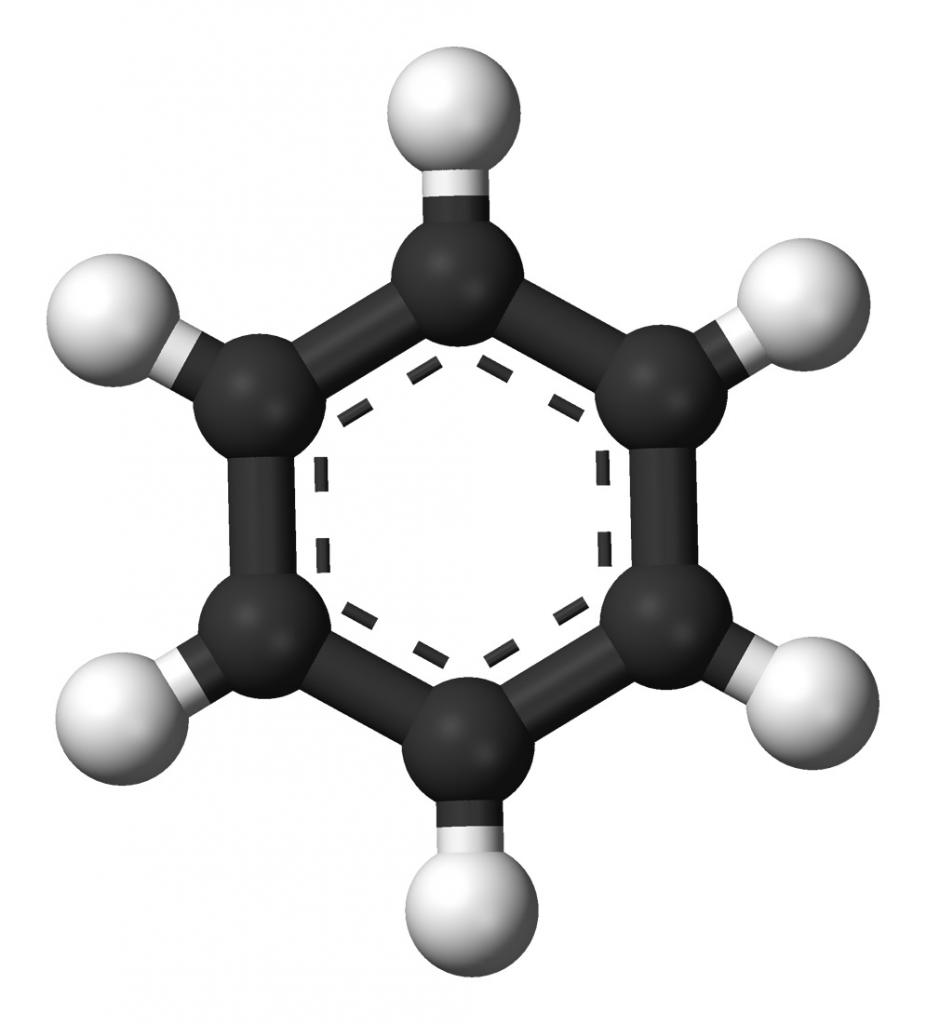
Простейшим представителем аренов является бензол. Молекулярная формула вещества – C6H6. Среди других ароматических углеводородов он имеет наиболее важное практическое значение. Соединение было обнаружено в 1825 году английским физиком М.Фарадеем в составе светильного газа. Оно представляет собой бесцветную жидкость, легче воды (плотность 0,88г/см3). Имеет характерный запах, ядовито. Температура кипения – 80, замерзает при 5,5. Физические свойства аренов, как и других органических веществ, зависят не только от качественного и количественного состава, но и от строения их молекул.
Загадка ароматического ядра
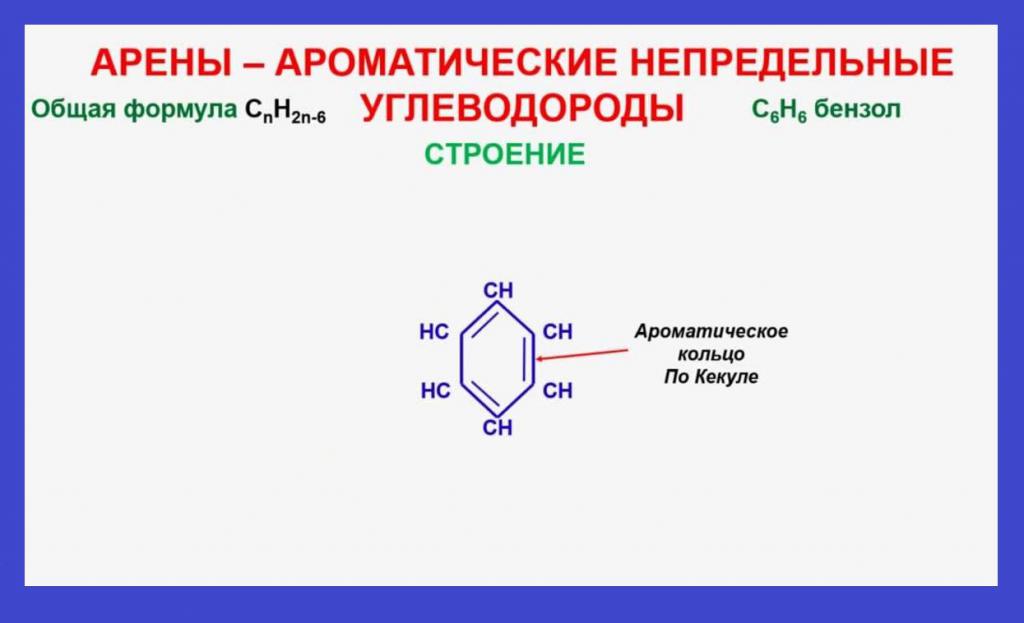
Первая структурная формула вещества была предложена немецким химиком Кекуле. В ней атомы углерода лежат в одной плоскости и образуют между собой правильный шестиугольник. Частицы карбона в молекуле соединены двумя видами ковалентных связей: одинарными и двойными.Однако, эксперименты не подтвердили наличие в бензоле пи-связей, так как вещество не окислялось растворами бромной воды и перманганата калия. Объяснением этого противоречия является электронное строение вещества. В его молекуле присутствует особый тип химической связи, названный ароматической или полуторной. Она представлена общим электронным облаком, состоящим из шести взаимно перекрывающихся p-электронов. Располагаясь над и под плоскостью молекулы, связь имеет вид кольца и называется ароматическим ядром. Полуторная связь обуславливает физические свойства аренов, а также их способность к реакциям замещения и присоединения.
Механизм процесса замещения
Система ароматического ядра имеет повышенную электронную плотность и может подвергаться атакам электрофильных частиц с дефицитом отрицательных зарядов. Итогом такого воздействия будет замещение атомов водорода на другие частицы, например, в молекуле бензола. Физические свойства аренов и особенности протекания химических процессов сильно отличаются от таковых у алканов или алкенов. Более того, в отличие от других классов органических соединений, арены нельзя описать одной общей формулой. Так, для нафталина формула будет иметь следующий вид: CnH2n-12, для бензола –CnH2n-6, для дифенила – CnH2n-14.
Хлорирование, бромирование и нитрование ароматических углеводородов происходит по единому механизму электрофильного замещения, в котором роль атакующего электрофильного агента играют анионы хлора, брома или нитрогруппы.
Почему реакции присоединения у аренов требуют жестких условий
Главная особенность строения молекул ароматических соединений заключается в наличии в их молекулах бензольного кольца, состоящего из шести перекрывающихся между собой p-электронов. От него зависят основные химические характеристики и физические свойства аренов. Для разрыва полуторной связи необходима дополнительная значительная порция энергии. Ее получают, применяя следующие параметры: ультрафиолетовое излучение, высокую температуру и давление в реагирующей смеси, а также используя катализаторы. Например, хлор присоединяется к бензолу только при облучении ультрафиолетовым светом, образуя гексахлорциклогексан (гексахлоран). Он применяется для протравливания древесины в процессе ее длительного хранения, а также в сельском хозяйстве в качестве средства для борьбы с насекомыми-вредителями.

C6H6 + 3Cl2 ---свет---> C6H6Cl6 - присоединение
Алкилбензолы
Если атомы водорода в молекуле бензола заместить углеводородными радикалами, например, метильным -CH3 или этильным -C2H5, то полученные ароматические углеводороды не будут являться простой суммой свойств алканов и аренов. Физические свойства и химические реакции, характерные для этих соединений, будут иметь ряд различий. Так, толуол и этилбензол являются бесцветными жидкостями со своеобразным запахом, более легкие, чем вода и нерастворимые в ней. Зато вещества хорошо растворяются в органических растворителях, например, ацетоне или дихлорметане. Их самих можно также применять в качестве растворителя. У ароматических углеводородов существуют и специфические характеристики. Поверхностное натяжение, коэффициент диффузии, вязкость – это физические свойства аренов, кратко описывающие их характеристику, как органических растворителей.
Нитрование ароматических соединений
Под действием азотной кислоты и в присутствии сульфатной кислоты в качестве катализатора арены подвергаются нитрованию. Реакция бензола с нитрующей смесью будет иметь следующий вид.
Нитробензол представляет собой маслянистую жидкость бледно–желтого цвета, имеющую характерный запах миндаля. Он применяется в качестве растворителя и служит исходным сырьем для производства анилина.
В реакции нитратной кислоты с толуолом образуется взрывчатое вещество – тринитротолуол или тротил. В качестве пирогенных соединений применяют и некоторые другие органические вещества с бензольными ядрами, содержащие кратные связи в боковых цепях.
Получение и применение аренов
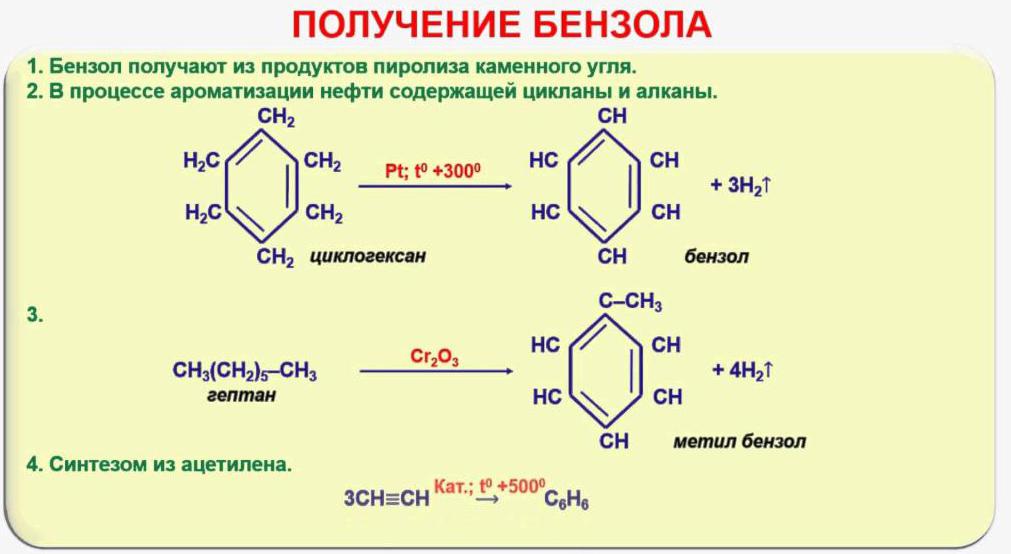
Физические свойства аренов: высокую теплоемкость, горючесть, способность растворять другие вещества, широко используют в различных хозяйственных отраслях. Бензол, толуол, нафталин, антрацен и другие ароматические углеводороды получают из нефти или каменноугольной смолы, образующейся в процессе коксования каменного угля. Так как потребность промышленности в аренах огромна, их добывают еще и способом каталитической ароматизации углеводородов, входящих в состав нефти и имеющих ациклическое строение. В этом случае происходит реакция дегидрогенизации – отщепление атомов водорода, в результате чего, например, из гексана можно получить бензол. В химии органического синтеза продолжают применять способ получения бензола из ацетилена. Реакция осуществляется при нагревании этина до 600° и называется тримеризацией. Химические и физические свойства аренов химия использует в процессах получения пластических масс, лаков, красителей.

Бензол применяют в качестве добавки к топливу. В сельском хозяйстве соединения - галогенопроизводные ароматических углеводородов, служат инсектицидами – средствами для борьбы с насекомыми-вредителями. Нитросоединения, например, тринитротолуол, применяют в военной промышленности в качестве взрывчатых веществ. Многие арены являются хорошими растворителями.
В нашей статье мы изучили химические и физические свойства аренов, и определили области применения этих соединений в промышленности.
Похожие статьи
- Арены: химические свойства и способы получения
- Физико-химические свойства толуола, уравнения реакций
- Органические соединения. Классы органических соединений
- Реакция Вагнера: механизм, роль в органической химии, применение
- Циклоалканы: химические свойства, применение
- Простые эфиры: свойства, получение, применение
- Получение фенола. Строение, свойства и применение фенола
